Expert Online GCP Training voor Klinisch Onderzoek in Europa
Deze training heette voorheen “Online EU-GCP training”. Leer alles over de Good Clinical Practice richtlijnen en Europese wetgeving van toepassing op klinisch onderzoek in Europa, via deze interactieve, gecertificeerde GCP training die je op eigen tempo online volgt. De training bestaat uit 7 interactieve online modules.
€ 175.00
Extra informatie
| Functie | Alle, Apotheker, Apothekersassistent, Klinische medewerkers onderzoekslocatie, Monitor/CRA, Onderzoeker, Onderzoekscoördinator, Onderzoeksverpleegkundige, Projectmanager, Sponsor/CRO-medewerkers, Studenten |
|---|---|
| Taal | |
| Niveau | |
| Fase | Afronding en archivering, Basis, Beoordelingsproces, Indiening, Opzet, Start onderzoek, Uitvoer, Voorbereiding |
| Regio | |
| Wetten en regels |
MEER DAN 5 LICENTIES NODIG?
LEERDOEL
- Principes van ICH GCP en het ICH GCP Addendum R2
- EU Richtlijnen 2001 & 2005
- Declaratie van Helsinki
- EU Privacy richtlijn (AVG)
- Rollen en verantwoordelijkheden in klinisch onderzoek
- Definities en afkortingen
- Onderzoeksprotocol ontwikkelen
- Selectie van onderzoekslocatie en -personeel
- Opzetten van kwaliteitssysteem: monitoring plan, auditen, DSMB, SOPs
- Overeenkomsten
- Beoordelingsprocedures en voorwaarden tijdens het onderzoek
- Rekrutering van proefpersonen en vereisten aan onderzoek met kwetsbare proefpersonen
- Veiligheid, inclusief rapportage van SUSARs
- Documentatie
- Voortijdige en reguliere beëindiging
- Afronden en archiveren van klinisch onderzoek
BESCHRIJVING
De volledig online EU GCP training is de perfecte oplossing voor cursisten die alles moeten weten over de Europese Richtlijnen en Good Clinical Practice, maar zelf hun tijd willen indelen. Tijdens deze training krijg je praktische inzichten in de Europese regels en GCP, in een logische volgorde vande opzet tot de afronding van klinische onderzoek.
Deze interactieve Europese GCP traning is ideaal voor CRA’s, onderzoekscoördinatoren, sponsors, onderzoekers, medewerkers van klinische onderzoekslocaties, apothekers, studenten en verpleegkundigen. Het stelt je in staat om klinisch onderzoek in Europa uit te voeren.
Bij je trainingslicentie krijg je 1 jaar lang continuous learning, waarmee je up-to-date blijft, ook als wet- en regelgeving verandert. Nadat je de training hebt voltooid, ontvang je het door Transcelerate erkende GCP Certificaat.
Schrijf je nu in en start met de myGCP training op je smartphone, tablet, laptop of computer.
TRAININGSINHOUD
Module: Introductie
- Inleiding in medisch wetenschappelijk onderzoek
- Typen klinisch onderzoek (interventioneel, therapeutisch, multi/singlecenter)
- Geschiedenis wet- en regelgeving klinisch onderzoek (Code van Neurenberg, Verkl. van Helsinki)
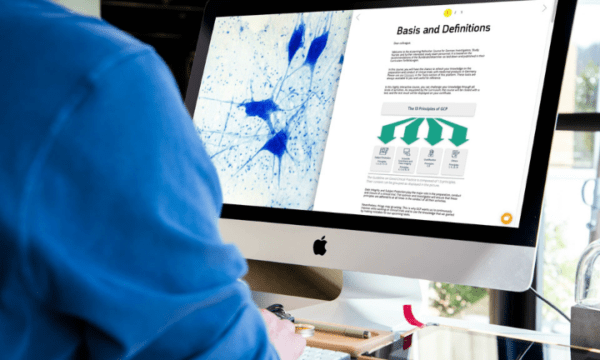
- De beginselen van ICH GCP, inclusief R2 Addendum
- Wet- en regelgeving klinisch onderzoek Europa (EU directives 2001 en 2005, EU Verordening 536/2014)
- De rollen in klinisch onderzoek (sponsor, toetsingscommissie, bevoegde instantie, monitor, auditor, onderzoeker, research professional)
- Extra eisen aan geneesmiddelenonderzoek
- Fases van geneesmiddelenonderzoek
- Begrippen en afkortingen in medisch wetenschappelijk onderzoek
Module: Opzet
- Protocol ontwikkeling en inhoud
- Selecteren onderzoeksteam
- Selectie van onderzoekers en onderzoekslocaties
- Selectiecriteria onderzoekers en onderzoekslocaties
- Opstellen en opbergen essentiële documenten (Investigator Site File)
- Risico-inventarisatie
- Kwaliteitsborging opzetten: monitoringplan, auditing, DSMB, SOPs
Module: Voorbereiding
- Onderzoeksproduct verpakken, etiketteren, invoeren en leveren
- Opstellen productinformatie (Investigators Brochure, IMPD)
- Opstellen patiënten informatie en informed consent
- Contracten en overeenkomsten
- Privacy wetgeving (GDPR)
- Verzekeringen (proefpersonenverzekering en aansprakelijkheid)
Module: Indiening
- Samenstelling standaard onderzoeksdossier
- Samenstelling en procedure toetsingscommissie
- Toetsing door ethische toetsingscommissie
- Toetsing door bevoegde instantie
- Beoordelingstermijnen en wijzigingen
- Toetsingsproces en goedkeuring
- Voorwaarden en verplichtingen na goedkeuring
Module: Start onderzoek
- Taken delegeren en initiatievisite
- Levering, opslag en gebruik onderzoeksproduct in een onderzoek
- Rekrutering van proefpersonen
- Informeren van proefpersonen
- Informed Consent procedure en toestemming
- Randomiseren en coderen
- Privacy van gegevens (GDPR)
- Eisen aan onderzoek met kwetsbare proefpersonen
Module: Uitvoer
- Amendementen, deviaties en wijzigingen in protocol en onderzoek
- Toevoegen van nieuwe onderzoekslocaties en onderzoekers
- Veiligheidsrapportages (AE/SAE/SUSAR)
- Veiligheid proefpersonen medische zorg en DSMB
- Documentatie en datamanagement (source, CRF, database)
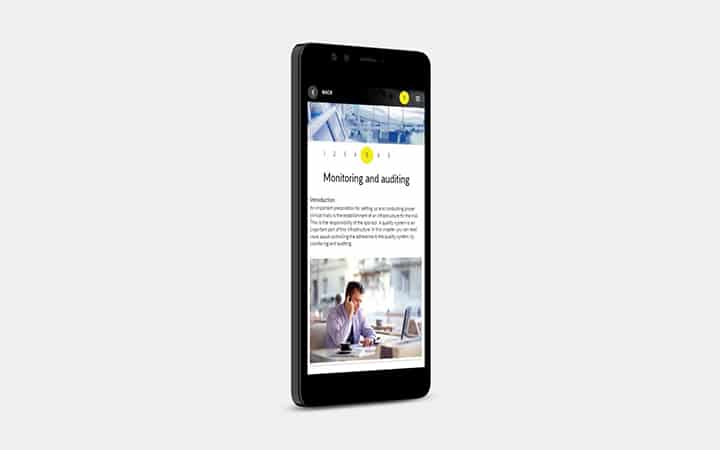
- Monitoring/Auditing /Inspectie
- Kwaliteitsborging en risico management (E6 R2 Addendum)
- Voortgangsrapportages
Module: Afronding en archiveren
- Afronding onderzoek
- Voortijdige beëindiging
- Melden einde onderzoek
- Eisen aan het eindrapport / Clinical Study Report
- Opslag en archivering onderzoeksdocumentatie
- Bewaartermijnen onderzoeksdocumentatie
ALTIJD EN OVERAL LEREN
LEER VOORTDUREND
VERDIEN JE GCP-CERTIFICAAT
Beoordelingen in alle talen weergeven (1)
Je moet ingelogd zijn om een beoordeling te plaatsen.
KEN JE IEMAND DIE DEZE TRAINING LEUK ZOU VINDEN? DEEL HET MET ZE…
KEN JE IEMAND DIE DEZE TRAINING LEUK ZOU VINDEN? DEEL HET MET ZE:
-

Expert ICH GCP Training voor Sponsors in Internationaal Klinisch Onderzoek
€ 99.00 -
GCP Refresher (AMG) Voor Klinische Geneesmiddelenonderzoeken In Duitsland
€ 199.00 -

Expert ICH GCP Training voor Sites in Internationaal Klinisch Onderzoek
€ 99.00 -

MDR Training voor Klinisch Onderzoek in Europa
€ 199.00







beoordelingen